La branca della chimica che studia le relazioni tra l’energia gli scambi energetici e le trasformazioni chimiche è la termochimica.
Nel caso in cui il calore sia l’unica forma di energia scambiata, definiamo esotermico un processo in cui l’energia sviluppata dal sistema è maggiore di quella assorbita ed endotermico il processo opposto.
Prima di iniziare ad analizzare gli scambi di energia nelle reazioni chimiche, è necessario conoscere alcuni termini usati in termochimica. Si definisce sistema quella parte dell’universo costituita da tutte le sostanze coinvolte nella reazione, sia reagenti che prodotti. Tutto ciò che si trova fuori dal sistema prende il nome di ambiente. L’unione di sistema e ambiente è detto universo.
In rapporto all’ambiente un sistema può essere:
- Isolato, nel caso in cui non scambia con l’ambiente esterno né l’energia né materia. Un liquido all’interno di un thermos è un esempio di sistema isolato, in quanto il thermos chiuso non consente scambi né di massa né di calore con l’ambiente, anche se per piccoli intervalli di tempo.
- Chiuso, se non può scambia re materia con l’ambiente esterno, ma soltanto energia. Una bombola di gas è un esempio di sistema chiuso, in quanto rispetto all’ambiente può raffreddarsi o riscaldarsi, ma non può cedere parte del suo contenuto.
- Aperto, nel caso in cui può scambiare con l’ambiente esterno sia materia che energia. Durante la combustione del carbonio per esempio il sistema scambia con l’esterno sia materia, che è il gas CO2, sia l’energia sottoforma di
Variabili Termodinamiche
Un sistema termodinamico risulta descritto da alcune grandezze che ne descrivono il comportamento globale del sistema,indipendentemente dalle caratteristiche individuali delle particelle che lo costituiscono.Esse sono:la pressione, la temperatura,il volume, energia di attivazione,l’entalpia e l’entropia. Quelle fra queste che risultano indipendenti sono dette variabili termodinamiche o variabil di stato. Le variabili termodinamiche si dividono in due categorie:
- variabili intensive: sono quelle variabili funzioni di punto, cioè che descrivono localmente il sistema; fra esse rientrano la temperatura, la densità, la pressione etc;
- variabili estensive: sono quelle variabili le quali descrivono il sistema nel suo complesso, come il volume, la massa, l’energia interna etc.
Il lavoro in Termodinamica
In un processo termodinamico i concetto di lavoro è simile a quello studiato in fisica. Immaginiamo di avere un gas a una data pressione, rinchiuso in un cilindro munito di stantuffo o pistone scorrevole. Per mantenere fermo lo stantuffo è necessario applicare sulla sua superficie una forza che faccia equilibrio alla pressione esercitata dal gas. Se,invece, la pressione interna del gas vince la forza esterna, il gas si espande sollevando il pistone verso l’alto e realizzando cosi un lavoro meccanico L il cui valore è dato dal prodotto della forza F per lo spostamento verticale ∆h dello stantuffo:
L=F·∆h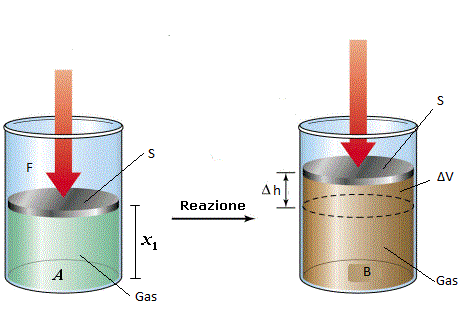
Ricordando che la pressione del gas può essere definita come il rapporto tra la forza F esercitata dal gas sulla superficie S dello stantuffo, si ricava:
F=p·S
Sostituendo nell’espressione del lavoro L, si ottiene:
L=p·S·∆h
Poiché
S·∆h non è altro che la variazione ∆V del volume dovuta all’espansione, si ha:
L= -p·∆V
Si può affermare che:
in un processo termodinamico che avviene a pressione costante, il lavoro è dato dal prodotto della pressione per la variazione di volume che ha luogo durante la trasformazione.
Trasformazioni irreversibili e Trasformazioni reversibili
Prendiamo di nuovo in considerazione un sistema materiale come quello del gas rinchiuso all’interno di un cilindro munito di pistone mobile. Abbiamo visto che il gas può subire una trasformazione che può manifestarsi come una compressione o una espansione. In entrambi i casi il sistema passa da uno stato 1 iniziale nel quale occupa un volume V1 ed esercita una pressione P1 a uno stato 2 finale nel quale entrambi i valori delle funzioni di stato P e V si sono modificati, diventando P2 eV2. Si dice allora che:
In un sistema termodinamico è avvenuta una trasformazione quando si può osservare una variazione di una o più funzioni di stato del sistema.
Una trasformazione, inoltre, può essere definita irreversibile o reversibile.
Consideriamo ancora un gas contenuto in un cilindro con stantuffo mobile. Se, per esempio, per consentire l’espansione del gas a temperatura costantrcostante togliamo uno togliamo uno per volta i pesetti posti sullo stantuffo, il processo che si realizza avviene per intervalli finiti, in modo rapido e irreversibile. Il lavoro L corrispondente alla trasfomazione che si realizza togliendo ciascun pesetto è rappresentato dall’area sottesa alla curva ottenuta nel piano p-V:
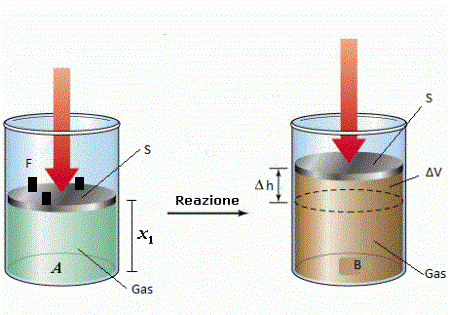
Il primo principio della termodinamica
Durante il processo chimico, il calore non è l’unica forma di energia scambiata. Consideriamo per esempio una reazione chimica, come quella dello stagno con l’acido cloridrico, fatta avvenire in un cilindro munito di pistone mobile.
L’idrogeno, che si sviluppa allo stato gassoso dentro il recipiente, si espande e solleva il pistone producendo lavoro, che si aggiunge al calore sviluppato. Ricordando che la pressione è espressa dalla relazione P= F⁄A e che il lavoro è definito come prodotto della forza F per lo spostamento s, L=F·s, si può ricavare per la forza l’espressione F=P·A e sostituirla nella formula del lavoro:
L=-P·A·s
Dal momento che il prodotto A·s corrisponde alla variazione di volume ∆V, cioè alla differenza tra il volume fiunale Vf e il volume iniziale Vi,dovuta all’espansione del gas prodotto a pressione costante, possiamo scrivere la relazione:
L=-P∆V = -P(Vf-Vi)
Il primo principio della termodinamica rappresenta una formulazione del principio di conservazione dell’energia e afferma che l’energia di un sistema termodinamico non si crea né si distrugge, ma si trasforma, passando da una forma a un’altra. Se si indica con Q il calore che il sistema scambia con l’ambiente circostante (che è positivo se viene assorbito dal sistema, negativo se invece è il sistema a cedere calore all’ambiente circostante) e si indica con L il lavoro (anche in questo caso il lavoro sarà positivo se si tratta di lavoro compiuto dall’ambiente sul sistema, negativo se è il sistema che compie lavoro), allora il bilancio energetico del sistema termodinamico, che rappresenta il primo principio della termodinamica, si scrive:

e si dice che la variazione di energia interna di un sistema termodinamico è uguale alla somma (algebrica) del calore e del lavoro entranti nel sistema. Il principio di conservazione dell’energia non distingue tra una forma di energia e un’altra (si può dire che esso coglie l’aspetto quantitativo dell’energia senza coglierne l’aspetto qualitativo). Se si riscalda un gas mantenendolo a volume costante – ponendo, per esempio, dei pesi sul coperchio a pistone di un contenitore per evitare che avvenga l’espansione del gas – il primo principio della termodinamica si riduce alla semplice uguaglianza:

poiché il gas non compie lavoro (L = 0) e il calore assorbito dal gas va ad aumentare la sua energia interna.
In una trasformazione adiabatica – compiuta, per esempio, isolando termicamente il gas, in modo che non vi sia alcuno scambio di calore con l’ambiente circostante (Q = 0), e diminuendo la pressione del gas (per esempio, togliendo man mano i pesi dal pistone che chiude il contenitore) – per espandersi il gas compie un lavoro (che sarà quindi negativo) e il primo principio della termodinamica si riduce all’uguaglianza:

Sempre in una trasformazione adiabatica, se si aumenta la pressione sul coperchio del contenitore, il lavoro (positivo) compiuto dal sistema uguaglia la sua variazione dell’energia interna, quindi:

Se, infine, si compie sul sistema una trasformazione isoterma (a temperatura costante) e si diminuisce la sua pressione, il gas si espande mantenendo invariata la sua energia interna, quindi per il primo principio della termodinamica si avrà:

L’entalpia nelle reazioni chimiche
Per esprimere il trasferimento di calore che avviene tra il sistema e l’ambiente in un processo che ha luogo a pressione costante,è utile introdurre una nuova grandezza termodinamica chiamata entalpia, che si indica con H ed è definita
H=E+pV
A pressione costante la variazione ∆H di questa grandezza sarà espressa allora dalla relazione : ∆H=∆E+p∆V
Pertanto possiamo dire che: Qp=∆H
Quando una reazione è condotta a pressione costante, il calore Qp, assorbito o ceduto, equivale alla variazione di entalpia ∆H del sistema.
Da questa uguaglianza si deduce che un processo chimico è:
- Endotermico, se Qp>0, quindi ∆H>0 e cioè H(prodotti)>H(reagenti)
- Esotermico, se Qp<0,quindi ∆H<0 e cioè H(prodotti)<H(reagenti)
Un semplice modo per ricavare i valori di ∆H di una reazione, consiste nell’adoperare una grandezza nota come entalpia di formazione standard
Si definisce entalpia di formazione molare standard di un composto, ∆H°, la variazione di entalpia quando una mole di composto si forma a partire dagli elementi nel loro stato più stabile, a pressione di 1 atm(atmosfera) e a 25°C
Il secondo principio della termodinamica
Dal primo principio della termodinamica abbiamo appreso che in qualunque processo di trasformazione di un sistema materiale l’energia si conserva sempre. Tale principio non ci dà alcuna indicazione sulla spontaneità di una trasformazione. Dal momento che qualunque sistema tende a raggiungere lo stato di minore energia a cui corrisponde la massima stabilità, per molto tempo si è pensato che l’esotermicità fosse il solo fattore determinante per stabilire se un processo può avvenire spontaneamente.A questo proposito nel 1870 il chimico francese Marcelin Berthelot (1827-1907) avanzò che le ipotesi che le trasformazioni che avvengono spontaneamente sono quelle che, nelle condizioni ambientali di temperatura e pressione, hanno luogo con sviluppo di energia termica.Tale criterio però non è sempre valido , in quanto esistono trasformazioni fisiche o chimiche che, pur essendo esotermiche, in condizioni ambientali non avvengono spontaneamente.Al contrario, esistono trasformazioni fisiche e chimiche endotermiche che, nelle condizioni ambientali, avvengono spontaneamente . Questo significa che il fattore energetico non è l’unico che interviene per determinare la spontaneità di un processo.C’è infatti un altro aspetto importante da considerare studiando qualunque processo di trasformazione: lo stato di disordine del sistema
Il grado di disordine di un sistema
Sono numerosi gli esempi della vita quotidiana che possono darci un’idea su ciò che intendiamo per disordine, un concetto apparentemente banale. Si ha un aumento di disordine anche nei passaggi i stato da solido a liquido e da liquido ad aeriforme. Lo stato solido è lo stato di aggregazione più ordinato, in cui le particelle si dispongono con ordine in figure geometriche raggiungendo il massimo livello di regolarità nei cristalli. Negli aeriforme, invece, il disordine è il massimo poiché tutte le particelle sono libere di muoversi irregolarmente e indipendentemente le une dalle altre.
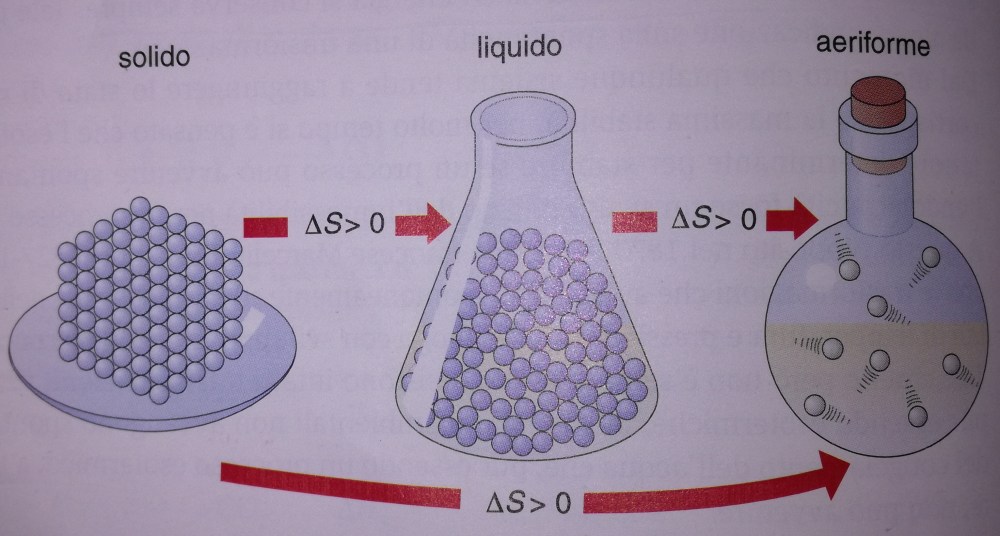
Sulla base di queste considerazioni è stato enunciato il secondo principio della termodinamica secondo il quale:
qualunque sistema isolato tende spontaneamente ad aumentare il suo grado di disordine.
Per applicare il secondo principio della termodinamica è necessario introdurre una nuova grandezza, l’entropia, che si indica con la lettera S e si misura in J/K. Tale grandezza ci informa sul grado di disordine di un sistema.
L’energia libera
Abbiamo appena appreso che qualunque trasformazione avverrà spontaneamente solo se, aumenta l’entropia dell’intero universo (sistema + ambiente). Pertanto, per poter utilizzare questo criterio è necessario effettuare misure tanto sul sistema quanto sull’ambiente. Se è facile però definire il sistema ed eseguire misure su quest’ultimo, la stessa cosa non vale per l’ambiente che, è definito come tutto ciò che circonda il sistema stesso. Per risolvere questo sistema è stato escogitato un modo di ricavare un criterio di spontaneità che si riferisce solo al sistema che, tiene conto anche del disordine dell’ambiente. A tale scopo è stata introdotta un’altra grandezza termodinamica, detta funzione di Gibbs o anche energia libera di Gibbs. Tale grandezza si indica con G, si misura in kJ/mol nel Sistema Internazionale(SI) ed è una funzione di stato. L’energia libera in realtà non è una nuova funzione termodinamica, bensì una conveniente combinazione dell’entalpia H e del prodotto tra l’entropia S e la temperatura assoluta T:
G=H-TS
Come per l’entalpia e l’entropia, anche per l’energia libera G ciò che interessa è la variazione delle grandezze coinvolte, più che i loro valori assoluti, per cui possiamo scrivere:
∆G=∆H-T∆S
Questa relazione, oltre a contenere grandezze facilmente misurabili perché riferite al solo sistema, fornisce un valido criterio di spontaneità delle reazioni chimiche a temperatura e a pressione costanti.
Infatti è possibile dimostrare che, in tali condizioni sperimentali, una reazione chimica avverrà spontaneamente se si accompagna a una variazione negativa della funzione di Gibbs:
∆G<0
Pertanto, un modo diverso e più utile di esprimere il criterio di spontaneità di una trasformazione è:
in un processo spontaneo che si svolge in un sistema chiuso, a pressione e temperatura costanti, G tende al minimo.