Gli atomi, quei corpuscoli che costituiscono la materia, sono quasi totalmente costituiti da vuoto e posseggono una struttura massiva definita nucleo, dove la materia è “stipata”. Nel nucleo sono presenti due tipi di particelle: protoni,carichi positivamente, e neutroni, che non sono dotati di carica elettrica ma tengono insieme i protoni nel nucleo come una colla . Attorno a questo nucleo sciamano a grande distanza e velocità particelle leggere cariche negativamente chiamati elettroni. Essi sono vincolati al nucleo tramite l’attrazione elettrica delle cariche positive dei protoni ma non vi collassano per via della loro altissima velocità e della loro piccolissima massa stimata come la duemilesima parte di quella del protone. Ad ogni protone esistente nel’universo è associato un elettrone (legge di conservazione della carica), quindi ogni elemento allo stato fondamentale ha un numero di elettroni che gli orbitano attorno al suo nucleo massivo uguale a quello di protoni nel nucleo.
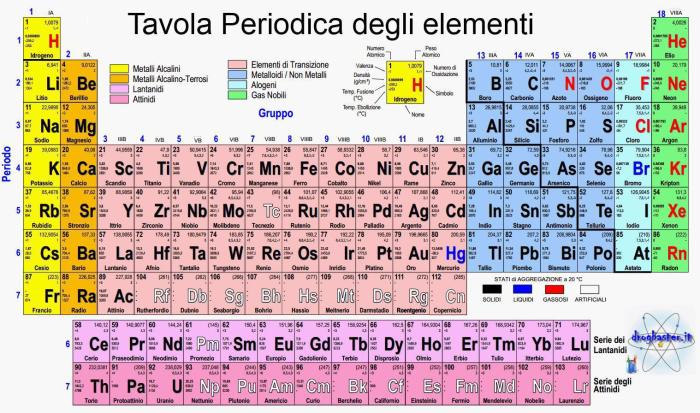
Il numero dei protoni determina le caratteristiche chimiche dell’atomo, la sua identità e la sua posizione nella Tavola Periodica. Gli elementi sulla tavola periodica sono ordinati (da sinistra a destra e dall’alto al basso) in base a questo numero, chiamato numero atomico ed indicato con la lettera Z. Atomi con numero di protoni diverso sono elementi chimici diversi. La Tavola Periodica moderna è una rivisazione, secondo le teorie più moderne, della prima organizzata da Dmitrij Ivanovič Mendeleev agli inizi del 900. La sua intuizione ha del miracoloso visto che non conosceva la struttura particellare dell’atomo, ma esso era ancora considerato indivisibile.
Legame chimico
Gli atomi sono “soggetti sociali”, non amano stare da soli e si legano tra loro formando molecole. Fanno eccezione gli elementi dell’ottavo gruppo della Tavola Periodica, i gas nobili, che posseggono una situazione ottimale per l’assetto elettronico, tale che sarebbe energeticamente svantaggioso formare molecole. Come si è potuto intuire, formare o meno un legame è questione di energia: le molecole tendono ad abbassare l’energia del sistema in cambio di stabilità. Gli elettroni, che sono le particelle con cui gli atomi interagiscono, sono disposti intorno al nucleo secondo regole ferree: si dispongono in livelli a crescente energia, in essi troviamo sottolivelli con orbitali in cui si possono collocare al massimo due elettroni che ruotano intorno al proprio asse (spin), come trottole, ma con rotazione opposta. La condizione energetica più desiderabile e, quindi, più stabile per un atomo è quella che gli permette di avere otto elettroni nel livello energetico più esterno, come per i gas nobili. Per tale motivo condividere o cedere elettroni ha una motivazione puramente utilitaristica.
Si ha un legame chimico quando una forza di natura elettrostatica tiene uniti più atomi in una specie chimica o più molecole in una sostanza allo stato condensato.
I legami chimici “più forti” hanno un contenuto energetico maggiore e sono più difficili da rompere, mentre i legami con minore energia hanno una forza minore e sono più facili da rompere. Da ciò deriva che le molecole che hanno al loro interno legami chimici più deboli sono più disposti a reagire. Inoltre tanto più un legame è forte, tanto minore è la lunghezza del legame, essendo la forza che tiene uniti gli atomi maggiore.
Legami primari
I legami chimici primari sono le forze che tengono uniti gli atomi che formano le molecole. Un legame primario è attuato dalla condivisione o dal trasferimento di elettroni tra atomi e dall’attrazione elettrostatica tra protoni ed elettroni. Tali legami generano il trasferimento di un numero intero di elettroni, detto ordine di legame, anche se in alcuni sistemi vi sono quantità intermedie di carica.
I legami primari sono generalmente classificati in tre classi, in ordine di polarità crescente:
Legame covalente
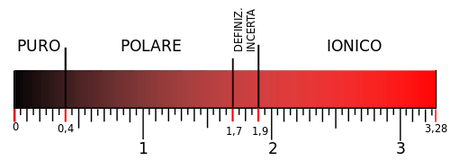
Il legame covalente è il legame che si instaura tra due atomi appartenenti ai non metalli (uguali o aventi differenza di elettronegatività – scala di Pauling – compresa tra 0 e 1,7) che mettono in compartecipazione una coppia di elettroni (detti coppia di legame) in un orbitale esterno che abbraccia entrambi gli atomi. Il legame covalente viene rappresentato da un trattino che congiunge i due atomi legati.
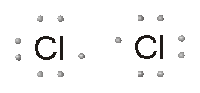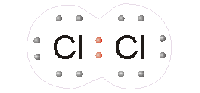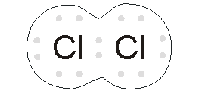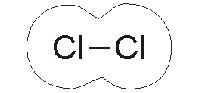
Qui a fianco vediamo ciò che accade all’interno della molecola di cloro. Ogni atomo condivide un elettrone con l’altro, creando una coppia di elettroni condivisa che terrà uniti i due atomi finché qualche forza esterna non li separerà.
Legame covalente puro
Un legame covalente puro (o apolare) e un legame che s’instaura fra due atomi appartenenti allo stesso elemento. In pratica si stabilisce una interazione tra atomi dello stesso tipo: è il caso tipico della molecola dell’idrogeno (H2) con un solo legame covalente omopolare, dell’ossigeno (O2) con due legami covalenti omopolari, dell’azoto atmosferico (N2) con tre legami covalenti omopolari.
Un legame covalente puro (o omopolare o apolare) si ha quando la differenza di elettronegatività tra due atomi è minore o uguale a 0,4. I legami covalenti che si formano fra due atomi che condividono due coppie di elettroni prendono il nome di doppio legame. I legami covalenti che si formano fra due atomi che condividono tre coppie di elettroni prendono il nome di triplo legame.
Legame covalente polare
Il legame covalente polare si instaura tra due atomi con differenza di elettronegatività compresa tra 0,4 e 1,7. In questo caso, gli elettroni coinvolti nel legame risulteranno maggiormente attratti dall’atomo più elettronegativo, il legame risulterà quindi polarizzato elettricamente, cioè ognuno degli atomi coinvolti nel legame presenterà una carica parziale. Tali molecole si comportano come dipoli, cioè piccole calamite, che si orientano in modo ordinato disponendo le estremità di segno opposto vicine.
Legame di coordinazione o dativo
È un tipo particolare di legame covalente detto dativo, in quanto i due elettroni coinvolti nel legame provengono da uno solo dei due atomi.
L’atomo che “dona” al legame la sua “coppia solitaria”, cioè entrambi gli elettroni appaiati presenti in un suo orbitale viene detto “datore”. L’altro, che mette a disposizione un orbitale esterno vuoto (cioè con due posti vuoti che possono essere occupati da due elettroni) o che riorganizza la sua configurazione elettronica per accogliere la coppia di elettroni (cioè ad esempio spostare due elettroni presenti su di un orbitale dispari su di un altro orbitale dispari, liberando di fatto un orbitale) viene detto “accettore”. Il legame dativo può essere rappresentato con una freccia, dal donatore all’accettore, o più impropriamente può essere indicato con un doppio trattino.
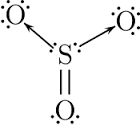
Legame metallico
La forma più estrema di delocalizzazione del legame covalente si ha nel legame metallico. Secondo questo modello un metallo può essere rappresentato come un reticolo cristallino di ioni positivi tenuti uniti da una nube di elettroni condivisi ed estesa a tutto il reticolo; essendo tali elettroni non legati a nessun atomo particolare, risultano essere estremamente mobili; tale mobilità è responsabile della elevata conducibilità elettrica dei metalli.
Legame ionico
Questo tipo di legame si realizza quando si legano elementi dalle proprietà chimiche molto diverse. Prendiamo come esempio il sodio e il cloro. Il sodio è un metallo, solido a temperatura ambiente e fortemente reattivo. Ha numero atomico 11, ha quindi 11 protoni e 11 elettroni, ma solo 1 nel livello energetico più esterno. Per raggiungere la stabilità deve perdere questo elettrone, raggiungendo gli otto elettroni nel livello inferiore. Il cloro è un gas, anche lui fortemente reattivo: ha numero atomico 17, il che vuol dire che ha 17 protoni nel nucleo e 17 elettroni, di cui 7 nel livello energetico più esterno. Deve acquistarne uno per essere stabile.
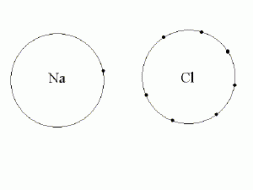
Qui di fianco sono disegnati i due atomi. A sinistra quello del sodio, con il suo elettrone esterno, e a destra quello del cloro con i suoi sette elettroni esterni. A questo punto tra i due atomi si realizza il trasferimento dell’elettrone, a causa dell’attrazione che il cloro esercita su quello del sodio, senza che questo si opponga alla sua perdita.
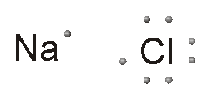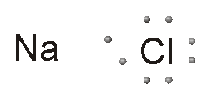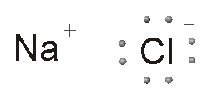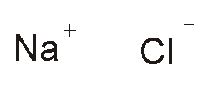
Quando questi due elementi si legano, il sodio cede il suo elettrone al cloro. In questo modo però si altera la neutralità elettrica dei due elementi: il sodio avrà una carica negativa in meno e diventerà uno ione positivo. Il cloro avrà una carica negativa in più e diventerà uno ione negativo. Il legame ionico è quel legame elettrostatico che si realizza tra ioni di segno opposto.
L’elettrone del sodio viene catturato dal cloro; il sodio diventa uno ione positivo e il cloro diventa uno ione negativo. Tra i due ioni si stabilisce un’attrazione elettrostatica che terrà legati i due atomi nel nuovo composto, il cloruro di sodio. Ma se vengono sciolti in acqua, liberano gli ioni e la soluzione diventa conduttrice (viene chiamata soluzione elettrolitica ogni soluzione in cui siano sciolti dei sali). I composti ionici non hanno una molecola vera e propria; la loro forma dipende dal numero degli ioni che si sono uniti.
Legami secondari
Questi legami sono esterni alle molecole, sono deboli, ma essendo molto numerosi in entità nanometriche ( 1nm=10-9 metri), sono responsabili di molti comportamenti macroscopici della materia . Un esempio sono i dipoli molecolari. Essi possono originare delle forze di attrazione intermolecolari. Un caso particolare di legame intermolecolare, che può anche essere intramolecolare quando la geometria della molecola lo consente, è il legame a idrogeno.
Un atomo di idrogeno legato ad un atomo di ossigeno (o di fluoro), instaura un legame eteropolare a causa forte differenza di elettronegatività e delle sue ridotte dimensioni. Su di esso si instaura una parziale carica positiva che attrae con un’intensità relativamente elevata gli atomi di ossigeno delle molecole vicine.
Tale legame, benché debole, è responsabile della conformazione spaziale delle proteine e degli acidi nucleici, conformazione da cui dipende l’attività biologica dei composti stessi.